GMPを勉強しよう(深堀りGMP5)逸脱に関する解釈

大体”deviations from…”という文脈になっています。”from”に続く単語は何か?探ってみましょう。すると、以下のような文章が続いています。
・specified proced ...
GMPを勉強しよう(深堀りGMP4)逸脱に関する解釈

「あれ、同じようなこと書いているな」と思いました。じほうの「GMP逸脱管理」という本です。私は「逸脱」の適用範囲を誤解している場面に何回か遭遇しました。それと同じようなことが書かれていました。
「製造部門の責任者は『手順書 ...
GMPを勉強しよう(深堀りGMP3)

解釈の道具は揃いました。あとは、どのように読んでいくかが課題です。
努力次第と書きましたが、「GMPの勉強のしかた」というのは、教わる場所がないように思います。勉強のしかたを教えることができる人は大勢いますが、大変なので誰 ...
GMPを勉強しよう(深堀りGMP2)-解釈のためのツール

私たちはこどもの頃に、交通信号の意味を習いました。青は進め、赤は止まれ、黄色は注意して進めでしたね。
おとなになった今、どのように解釈していますか?
ところで教習所の教材以外に、道路交通法施行令を読んだことあり ...
GMPを勉強しよう(深堀りGMP1)

「深堀り」とは言ってみたものの、それほど深くないなと感じました。やや深堀りって、変な表現ですね。どうしよう。
何を述べたいかというと、「GMP要件の解釈のプロセス」をたぐり出したいということです。それを繰り返すことによって ...
ちよだ事務所を引き揚げました

足掛け7年入居していたちよだプラットフォームスクエアから引き揚げました。書類上は3月末日まで入居していますが、一昨日手続きを終了しました。
仕事は自宅事務所で処理できるので、コロナ禍になってからはほとんど足を向けていません ...
PIC/S GMP ANNEX 1 の内容に関する考察-1

WFIシステムのデッドレグは3d以下ですか?それとも6dルールを採用したシステムですか?
無菌製剤を製造している製造所では、PIC/S GMP ANNEX 1の改訂で少なからず影響を受けていると思います。改訂からすでに1年 ...
「グローバルGMP講座」と「GMP監査員養成講座」の日程が決まりました
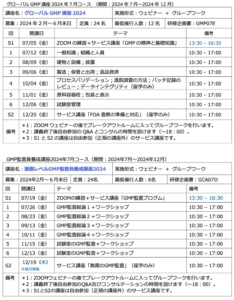
久しぶりにブログを書いています。外に向けて書いていると、昨年の秋ごろから今まで遠野のカッパよろしく水面下にいたような感じがします。今、少し顔を出したかな…って感じです。仕事も関係してたんですが、閉じこもりが長かったかな。 ...
M2 Macbook Airどうかな?

1つ仕事が終わったので、Macbook Air を注文しました。以前からAppleのバッグに入れていたのですが、なにかけじめがついてから買おうと思って、今日注文しました。3日で着くって。
仕事にマッチングするPCかどう ...
GMP監査員養成講座 5回目無事終了しました

GMP監査員養成講座 5回目無事終了しました。ご出席された皆様、ありがとうございます。お疲れ様でした。
今、機材の片付けを終えて、このブログを書いています。今日は質問が1つでした。少し時間をかけて回答しました。GMP省 ...









