GMP査察

査察対応プロジェクトの重要成功要因を一つだけあげるとしたら、「よいマネジメントサイクルを回すこと」だと思います。具体的には、柔軟でち密な総合計画の策定、チームの組織化と育成、一致協力してプロジェクトを進行させ、継続的な進捗管理をおこなうことです。重要活動計画には、主要手順書と(できれば)過去3年間の記録と報告書のレビュー、役割演習による質疑応答トレーニングなども盛り込まれているとよいでしょう。
-
システム査察
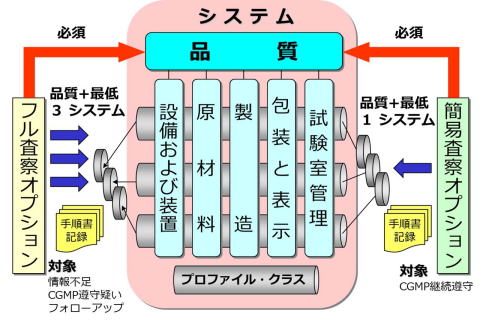
FDA査察は、PAIも含めてシステム査察を実施しています。システム査察は、特定の製品のGMP遵守ではなく、当該製造所全体のGMP遵守を評価するアプローチです。そのため、GMP査察を受けるために必要な知識として、システム査察の概要および査察の焦点などをまとめました。
システム査察は、GMPの実践領域を6システムに分けて、剤型や製造工程によって分類された、医薬品のプロファイルクラスを横断的に調査し、当該製造所のGMP遵守状況を評価します。この結果は、各製造所のプロファイルに収められます。FDAが製造所を評価する際、約3年間さかのぼって、その結果を参考としています。
上のボタンをクリックするとGMP査察の関連投稿記事がご覧になれます。