FDA Warning letter 320-17-38(品質システム、手順書、データインテグリティ)

FDAのWarning letterが掲載されました。
医薬品GMPに関するFDAのWarning letterを紹介します。今回の対象会社は、中国のAPI製造施設です。
品質システムが構築されていないこと、手 ...
FDA Warning letter −320−17−25(データインテグリティ)

このところ、FDAのWarning letterが続々掲載されています。追々、内容を紹介していきたいと思いますが、本日は安定性試験における「データインテグリティ」の問題が指摘された例を紹介します。
今回の対象会社は、中国の ...
GMPを勉強しよう‐57‐データインテグリティ管理手順
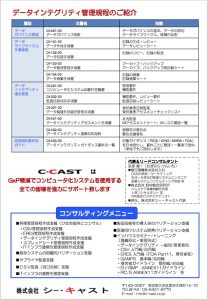
先週、ある委員会に出席していたら、こんなコピーを受け取った。内容は、「データインテグリティ管理規程の紹介」というもので、こちらのページは裏面。有名な荻原さんがまとめた資料で、データインテグリティを管理していくための一式が揃っている。
FDAのWarning letter(無菌製剤の粒子汚染)WL320-17-19

医薬品GMPに関するFDAのWarning letterを紹介します。今回の対象会社は、イギリスの無菌製剤の製造施設です。筆頭に上げられている欠陥は、「粒子の汚染」でした。この査察は2016年に実施されましたが、2015年の査察でも同 ...
FDAのWarning letter(API再包装)WL#320−17−14

医薬品GMPに関するFDAのWarning letterを紹介します。今回の対象会社は、中国のAPI製造施設です。再包装作業に関する指摘事項です。
■ホームページアップデート日:20170118
WL#: 320- ...
EMAのNon-compliance Report(ワクチン)-DICM/INSP/AMG/MBP/ACS

このNon-Compliance Reportは、スペイン当局から発行されました(発行日2016年12月5日Report No : DICM/INSP/AMG/MBP/ACS)。対象の会社は、スペインの医薬品製造業者です。
EMAのNon-compliance Report(再包装)-DK H 00083517

このNon-Compliance Reportは、デンマーク当局から発行されました(発行日2016年12月13日Report No : DK H 00083517)。対象の会社はデンマークの”EuroPharma.DK ApS”で、医 ...
FDAのWarning letter(無菌API)20170105

FDAのWarning letterが掲載されました。
今回の対象会社は、インドの無菌原薬製造施設です。無菌APIの指摘は、久しぶりですね。無菌APIは、製剤と同等のGMPが適用されますので、指摘事項には製剤GMPのセクシ ...
データインテグリティに関する問題について

データインテグリティの問題が発見されると、かなり早い時点でWarning letterが発行されているように感じます。最近の例では、FDA査察が2016年6月に実施されました。会社側の回答は、期日を守って7月8日に提出されています。そ ...
ジェネリック・スキャンダルとデータインテグリティ

欧米当局の査察で顕著に見られるトレンドは、「データインテグリティの問題」の急増です。この状況を懸念して、FDAは医薬品製造業者の監査者に対しても、供給業者の監査でデータインテグリティの問題のレビューを期待しています。
品質 ...









