FDA Warning letter 320-20-08

今週のWarning letterなんですが、
海外査察(CDER発信)では、先週出された2通のWarning letter(320-21-07と320-21-09)の間の番号320-21-08が掲示されました(ニコッ)。 ...
FDA Warning letter(320-20-47):

世界的なコロナ禍においても、CDER管轄(米国外)Warning letterだけでも50近く発行されています。2000年前((・.・;):西暦2000前すなわち1990年代です。)の厳しさに戻ってきた感があります。
ちな ...
FDA査察が再開したら、こんなことに注意しましょう!FDAガイダンスの紹介

FDA査察が再開されたら、このガイダンスに記述されたことはレビューされる可能性が高いと個人的に感じました。そのため、皆さんに注目していただきたく、紹介します。
新しく発行された以下のガイダンスは、即施行されます。
FDA Warning letter (320-20-40):API(カナダ):経営陣の監督

(“..)φ:また出ましたね、”management oversight”。しかし今回は文章中ではなく、1項目とって(と言ってもAPIなので、適用セクションの項目はないのですが)太字で書かれています ...
FDA Warning letter: API(インド);溶剤の回収

今回の対象会社は、インドのAPI製造施設です。
指摘は、1)溶剤の回収; 2)装置の洗浄; 3)データインテグリティに関する3項目です。
データインテグリティは永遠のテーマなのでしょうか?
今回は、 ...
FDA Warning letter(320-20-36):OTC(カナダ):データインテグリティ;OOS調査

医薬品GMPに関するFDAのWarning letterを紹介します。今回の対象会社は、カナダのOTC医薬品製造施設です。
指摘は、1)試験記録(DI); 2)試験法; 3)安定性試験; 4)OOS調査に関する4項目です。 ...
オンラインウェビナーのイメージ更新しました。

少しずつウェビナーに慣れてきました。まだまだ改善すべき点はありますが、なんとかここまでやってきました。
そこで、ホームページのウェビナーのイメージを更新しました。
6月12日に実施した「QA監督」の一部を切り抜 ...
「FDA-483回答のしかた」のウェビナーを実施しました。

ご出席者の皆様、ありがとうございます。
登録者全員、無事参加できました。オーディオもうまく機能したみたいです。
FDA-483の回答に関しては、コンサルテーションとして、または社内セミ ...
経営陣の責任とは

医薬品品質システム(ICH Q10)で経営陣の責任を述べていますが、そこから始まったわけではありません。経営者は株主の利益のために行動すると同時に、組織の遵法経営の責任を有していることは言をまたないところです。
(R ...
職務記述書のスキーム
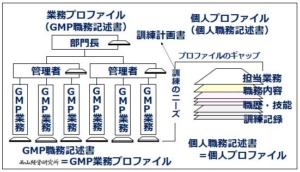
職務記述書のスキーム作りました。








