EMA Non-Compliance Report(DE/NCR/MP/2/2017)ドイツ当局;データインテグリティ他

このNon-Compliance Reportは、ドイツ連邦オーバーバイエルン当局から発行されました(発行日2017年8月8日Report No : DE/NCR/MP/2/2017)。対象の会社は、インドの医薬品製造業者です。
EMA Non-Compliance Report(UK MIA 17907 Insp GMP 17907/13988-0025 NCR)データインテグリティ

このNon-Compliance Reportは、英国当局から発行されました(発行日2017年8月24日Report No : UK MIA 17907 Insp GMP 17907/13988-0025 NCR)。対象の会社は、英国 ...
FDA Warning letter(320-17-43)中国の会社:品質部門、バッチ記録、出荷判定試験など

FDAのWarning letterが掲載されました。医薬品GMPに関するFDAのWarning letterを紹介します。今回の対象会社は、中国の医薬品製造施設です。
WL#: 320-17-43
日付: Aug ...
FDA Warning letter Case #515029(作業の分離、品質監督、試験)

FDAのWarning letterが掲載されました。
今回紹介する警告書の対象会社は、アメリカ ウィスコンシン州のOTC製造施設です。医薬と非医薬の作業の分離、品質監督、試験未実施(というかデータの捏造)が指摘されていま ...
簡潔、明快、具体的で実践的なセミナーです

日米欧のセミナー参加者のアンケート結果は、いずれもトップレベル!
講師のJohn Y. Leeは、ダントツの評価を得ているトレーニングの専門家です。元FDA査察官で、製薬会社で品質保証部長も努めた、官民の経験豊富なトップコ ...
FDA Warning letter(ホメオパシー医薬品)17-NWJ-09

FDAのWarning letterが掲載されました。過去に他社で健康被害が生じたホメオパシー医薬品(幼児用のteething tablet)の警告書です。
WL#: 17-NWJ-09
日付: June 20, ...
バッチ記録の照査のスライドで、こんなのがありました。

バッチ記録の照査のスライドを整理していたら、こんなのがありました。社内セミナー用にアレンジしたスライドです。
電子文書管理システムでは、あまり起こりそうにありませんが、手書きで紙ベースのバッチ記録では、起こることがあるかも ...
FDA Warning letter 320-17-38(品質システム、手順書、データインテグリティ)

FDAのWarning letterが掲載されました。
医薬品GMPに関するFDAのWarning letterを紹介します。今回の対象会社は、中国のAPI製造施設です。
品質システムが構築されていないこと、手 ...
FDA Warning letter −320−17−25(データインテグリティ)

このところ、FDAのWarning letterが続々掲載されています。追々、内容を紹介していきたいと思いますが、本日は安定性試験における「データインテグリティ」の問題が指摘された例を紹介します。
今回の対象会社は、中国の ...
GMPを勉強しよう‐57‐データインテグリティ管理手順
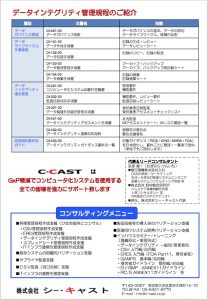
先週、ある委員会に出席していたら、こんなコピーを受け取った。内容は、「データインテグリティ管理規程の紹介」というもので、こちらのページは裏面。有名な荻原さんがまとめた資料で、データインテグリティを管理していくための一式が揃っている。








