GMP遵守に関する企業の格付け‥.国の格付け
FDAは、企業から提出されたデータをもとに、品質メトリクスを計算して、同じ尺度で企業の格付けを図ろうとしています。現在はドラフトガイダンスの段階ですが、これが最終版になると、データの提出が要件化されます。
この格付けは、査察のスケジューリングに使われるもので、FDAの負荷を低減するためにおこなうことをドラフトガイダンスで述べています。現在のFDA査察のスケジューリングは、FDAが持っている情報をもとにしたリスクベースアプローチでした。しかし、これからは同じ指標で評価した事業所の格付けも加わると思われます。
ところで、FDAからみた日本企業のGMP遵守レベルはどの程度なのでしょうか?もちろん、インドや中国よりも遥かにいいはずです。しかし、FDAが発表している情報をまとめてみると、意外なことが見えてきました。
そこで、自分なりにまとめてみた数字を紹介します。
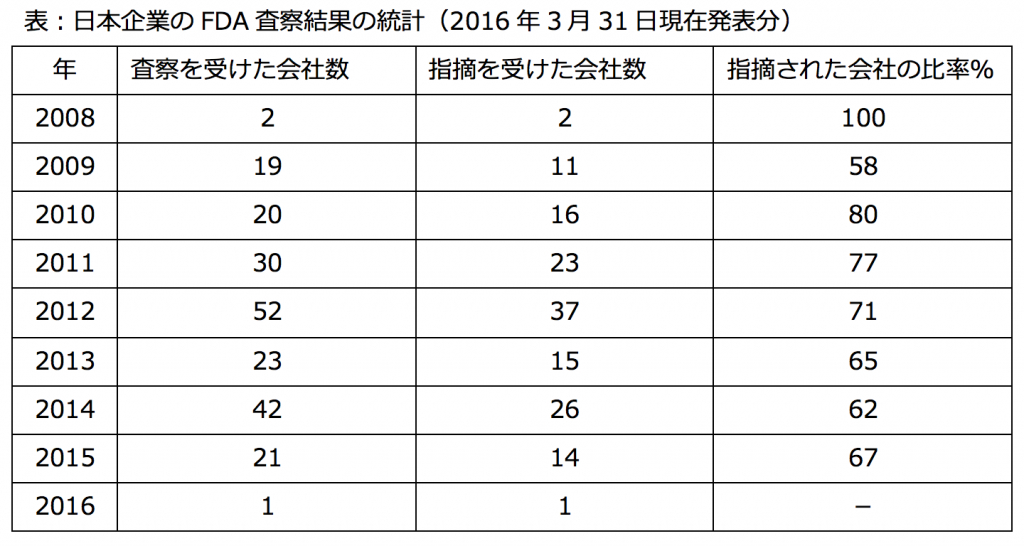
日本は、査察件数が比較的少ない国です。このあとの表で比較した国別でみると、英国の査察件数が最も少なく、ついで日本です。インド、中国は大変多くの会社がFDA査察を受けています。
重要かつ明確なGMP違反の指摘(FDA-483)を受けると、FDAが分類するVAIまたはOAIに入ります。VAIは、重要なGMP違反を会社が自主的に改善して報告することを求めている分類です。OAIは、重要なGMP違反を自主的な改善に任せず、規制措置を実施する分類です。いずれにしろ、FDA査察時点で、米国GMPを遵守していない点が見つかったことを意味します。簡単に言うと、VAIは不合格だけど追試を受けさせてもらえるが、OAIは不合格でそのまま落第ということです。
その他に、NAIという分類があります。これは、重要なGMP違反がなかったことを示す分類です。FDA-483がでなければ、まず合格は確実ということです。
ちなみに、FDA-483は重要なGMP違反が明らかに存在する場合、FDA査察官がそれをリストして、査察終了後に発行する書類です。この「重要」は"significant"で、私達が普段使っている「重大」なGMP違反の"critical"とは異なります。EUが評価する"critical"は、1件でもあればNon-Complioance reportがEU諸国に通知されます。私達が「中程度」と称している違反は、EUでは"major"にあたるものだと思います。"major"が5〜6件観察されれば、"critical"と判断されます。
統計では、FDA査察を受けた日本企業の60〜70%が、指摘を受けています。この件数は、やや減ってきているように思えますが、有意差は見られません。米国は大中小零細にいたるまで、全ての会社がFDA査察を受けていますが、指摘される比率は50%前後で毎年変わりません。すなわち、FDA査察は合格率50%の試験のようなものです。
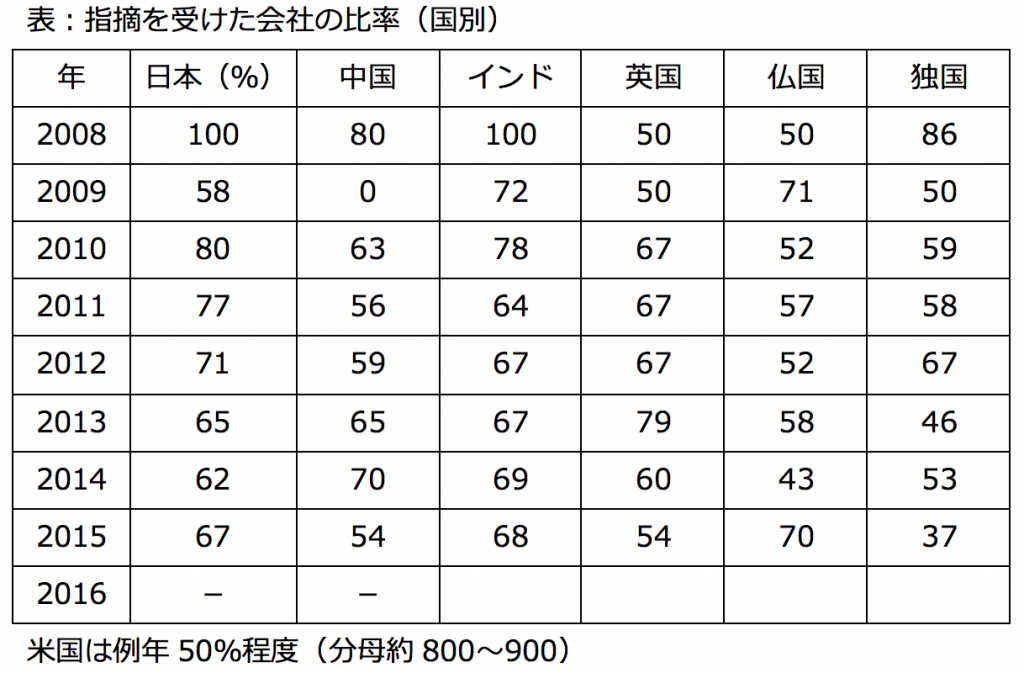
アジア、ヨーロッパの国と比較してみました。日本は、中国、インドに比べてOAIは少ないものの、合格率はたいして変わりません(中国の方が若干よいですね)。これが現状です。ヨーロッパは、フランスが米国より少し劣る程度です。ドイツもほぼ同じレベルです。英国は、ヨーロッパの中では最も悪い成績でしたが、過去3年は良くなっています。
FDA-483への回答のコスト(人、時間、機会損失)は、無視できません。FDA-483をもらうのは当たり前と考えず、できれば追試なしで一発合格したいものです。

