PIC/S GMP 講座-7 1.5-1.6 品質リスクマネジメント

このセクションは品質リスクマネジメントについての要件です。リスクマネジメントをどの手順に適用するのかを説明します。
以下のタイトル(画像)をクリックして、動画をYouTube から視聴することができます。
PIC/S GMP:1.2-1.4 医薬品GMP・品質管理・製品品質照査

GMPと品質管理は、ちょっとまとめただけのセクションです。製品品質照査はアメリカのいわゆる年次照査と異なりますので、要注意です。品質照査の対象項目を確認しましょう。
今回から、画像 ...
今週のWarning letter 13/10/08

今週は医薬品GMPに関する警告状は発表されませんでしたヽ(^。^)ノ
FDAのアップデートはどうなる?
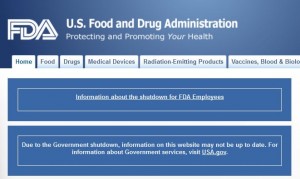
今アメリカは大変なことになってる。政府がシャットダウンしているので、FDAのホームページを見たら、こんな表示です。
今週のWarning letter 13/10/01

今週は医薬品GMPに関する警告状は発表されませんでしたヽ(^。^)ノ
今週のWarning letter 13/09/24

今週はWarning letterが3通掲載されました。インドの会社が2社、1社は原薬、1社は無菌製剤です。残りの会社は、プエルトリコの工場ですが、Warning letterのあて先はドイツの親会社のCEOで、CCとしてアメリカの子 ...
3分間PIC/S GMP講座-5 品質マネジメントの原則と品質保証1.1

3分間PIC/S GMP講座-5 品質マネジメントの原則とセクション1.1品質保証
いよいよスタートです。
以下のタイトル(画像)をクリックして、動画をYouTube から視聴することができます。
今週のWarning letter 13/09/17

今週は医薬品GMPに関する警告状は発表されませんでしたヽ(^。^)ノ
読んでおきたい査察対応のための本

FDA査察の生々しい現場の情報を書いた本:FDA査察
書き下ろしと言ってもよいぐらいの本です。 経営者の方にも読んでいただきたい本です。
本日開局!

本日、スタジオGMPの1チャンネルを開局しました。このチャンネルは、GMPにまつわる「よもやま話」を載せる予定です。いろいろな人と会って、いろいろ話して、本で読めない面白い話、ためになるけど無駄話みたいなものを紹介したいと思います。









