QA監督(品質監督:Quality Oversight)の公開セミナー案内

QA監督または品質監督という言葉を聞いたことはありますか?FDASIAで出てきた言葉ですね。
QA監督とは何をするのか、なかなかはっきりしていません。FDAはCGMPでQAの役割や責任は求めている物の、QA監督に関するガイ ...
FDAのWarning letter(#320-16-08)-2016年3月16日FDAホームページ掲載

医薬品GMPに関するFDAのWarning letterが1通掲載されました(2016/03/16 ホームページ掲載)。今回の対象会社は、インドの無菌製剤の工場です。
その他、調剤薬局のGMP違反に関するWarning l ...
GMPを勉強しよう−35-リスク評価
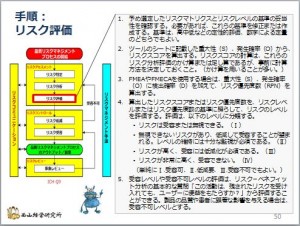
リスク分析をしたら、次のステップはリスク評価です。ここまでがリスクアセスメントの段階です。
僕がICH Q9を読んでいてふと思ったことがあります。
リスク分析で点数付けすると、リスク評価とリスク受容の判断(低減 ...
FDAのWarning letter(#:2016-DAL-WL-12)-クリーニング手順

前回に続き、クリーニング手順の具体的な指摘内容を見ていきましょう。
クリーニング手順:
貴社のクリーニングと消毒方法が適切であること、または日焼け止めと抗真菌製品を含む局所剤の製造に使用された非専用装置を保証し ...
GMPを勉強しよう−34-なぜFDA-483なの?

今回は、演習問題です。
一人で解いてもよいですが、できればグループディスカッションまたはケーススタディ用の演習問題として、話し合っていただければと思います。
なお、演習問題には回答(または講評)はつけないつもり ...
FDAのWarning letter(#:2016-DAL-WL-12)-水システム

この警告書は、情報は以下の通りです。FDAのホームページには、3月10日に掲載されました。今回は指摘番号2の「水システム」について要約します。
—————————————
WL#: 2016-DAL-WL-12
FDAのWarning letter-製剤(局所剤)-2016/03/10 ホームページ掲載

FDAのWarning letterが1通掲載されました。(2016年3 月10 日)
医薬品GMPに関するWarning letterが1通掲載されました。(2016/03/10 ホームページ掲載)今回の対象会社は、ア ...
GMPを勉強しよう−33-QRM-リスク分析
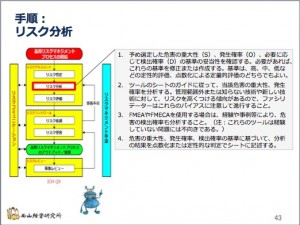
リスク特定、すなわち「ハザードのリスト化ができたら、次はリスクの分析です。左図のフローチャートのリスクアセスメントの段階のうち、赤枠のところが「リスク分析」のステップです。
ぼくの作成した手順は、例によって ...
GMPを勉強しよう-32-CGMP:治験薬から承認前査察まで

5月20日の公開セミナーのテーマが決まりました。「CGMP:治験薬から承認前査察まで」です。
FDAは治験薬GMPを規則(Regulation)として持っていません。ガイダンスが出ていますが、それ ...
GMPを勉強しよう-31-EMA査察の観察事項の格付けイメージ

EU査察の観察事項は、個別にクリティカル(Critical)、メジャー(Major)、アザー(Other)に分類される。単純比較はできないが、日本流に言えばそれぞれ重大、中程度、軽微となるかもしれない。
ちなみにFDA査察 ...








