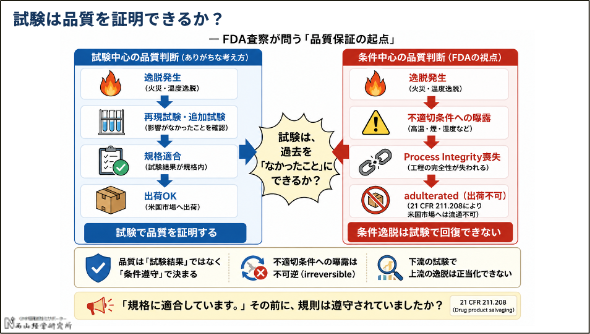
「試験は品質を証明できるか」‐ FDA査察から見た目のつけどころとチェックポイント
今回のWarning Letterは、インドの原薬(API)メーカー、Macsen Drugsに2025年3月5日付で発出されたものです(Warning Letter 320-25-51)。
URL:https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/warning-letters/macsen-drugs-698202-03052025 (原文は英語ですが、ブラウザの翻訳機能を使うと日本語で読むことができます。)
査察は2024年9月に実施されました。FDAはそこで、2022年12月に工場内で発生した火災への対応を問題にしました。火災の影響を受けたブロックに保管されていた原薬は、高温や煙に曝露されたにもかかわらず、品質部門が米国市場向けに出荷していたのです。
この会社はFDA 483への回答として、「火災時の状況を再現した試験により、製品への影響はなかった」と結論づけました。これに対するFDAの反応は明快でした。
「あなたの回答は不十分です。不適切な保存条件にさらされた医薬品は、すでに不純物混入品(adulterated)とみなされ、米国市場への流通には適しません。」
また、この会社のインシデント報告書に「劣化した」と記載されたロットが、市場回収の対象とされていなかった点も問題視されました。
GMP省令やPIC/S GMP Part IIでも、保管条件の維持が求められており、その規格に適合しないものは出荷できません。しかしGMPを読んだだけでは、火災の影響を受けた製品が「不適合品」と明確に位置づけられているわけではありません。そのため現場では、「試験して規格内であれば問題ない」と判断してしまうことはないでしょうか。
しかし、FDAが問うのは試験結果ではありません。「製品がそもそも適切な条件下に置かれていたか」という工程の完全性(Process Integrity)です。
あまり馴染みがないかもしれませんが、FDAの21 CFR 211.208(医薬品の救済)は、当該製品を出荷できないことを明確に規定しています。この要件を満たすためには、試験は重要ですが、それだけでは十分ではありません。すなわち、不明な保管条件の影響をすべて試験で証明することは困難である、という前提に立っています。
“Drug products that have been subjected to improper storage conditions including extremes in temperature, humidity, smoke, fumes, pressure, age, or radiation due to natural disasters, fires, accidents, or equipment failures shall not be salvaged and returned to the marketplace."
ここで、査察官の思考プロセスを推論してみます。
火災の影響を受けたロットが出荷されていた
→ QUはなぜ出荷を止めなかったのか?
→ 事後の再現試験の結果に依拠した判断をした
→ しかし、不適切条件への曝露はすでに発生している
→ 試験はその事実を「なかったこと」にできるのか?
→ 曝露した時点でadulteratedとみなされる可能性が高いので、「なかったこと」にできない
→ 根本原因:品質保証の起点が「条件の適切性」ではなく「試験結果」に置かれている構造
この指摘の本質は、試験の精度の問題ではありません。「何をもって品質と見なすか」という品質保証の構造そのものにあります。FDAは、「下流の試験で上流の逸脱を正当化することはできない」という立場を一貫してとっています。
この構造が変わらない限り、同様の判断は繰り返されるリスクがあります。
私たちは、製造または保管条件に逸脱が生じたとき、最初の一手が「試験して確認しよう」になっていないでしょうか。その出発点が、FDAの視点とは少しずれている可能性があります。
ICH Q7やGMP省令を読むことは重要です。しかし、FDA査察に対応する場合、それだけでは十分とは言えません。FDAのCGMPにおける「C:Current」は、条文・ガイダンス・Q&A、そしてWarning Letterを含めた、FDAの経験に基づく“生きた基準”です。GMP省令で言えば「その他所要の措置」に相当する考え方です。
21 CFR 211.208に「fire」という一語が明記されている事実は、「FDAの条文を自分の目で読む」ことの重要性を、私たちに教えてくれているように感じます。
「規格に適合しています。」その前に、規則は遵守されていましたか?
◇◇~~~~~~2026年度公開セミナーのご案内~~~~~~◇◇
◆国際レベルGMP監査員養成講座の案内書
◆グローバルGMP講座の案内書