FDAが関心を示しているQuality Metrics(品質測定)の項目は?
FDA査察のために統合された新たな組織は、品質測定プログラムを重要要素の一つと位置づけている。FDAはこれを見ることで、その会社のGMP遵守の程度がどのあたりにあるかを判断するのだろうか?そうすれば、今までの「OAI、VAI、NAI」の3段階の評価よりも緻密な評価ができるようになるということなのだろうか?一種のリスクアセスメントといえるかな。一体何をおこなったら対策になるのだろう?
これらは、個別の具体的な対策をとれば達成するというものではない。品質システムを継続して効果的に実施していくしかないと思う。すなわち日頃の実践が大切だ。品質目標を達成するための品質計画を策定して、継続的に実行とモニタリングをしていくことかな?個人的にはこのように思う。
今までFDAが品質測定の候補となるものを議論してきた結果 、次のものに注目しているとECAのニュースがまとめていた。それは、FDAスタッフが発表した次のスライドと同じ内容だった。
簡単にまとめると、こんな感じの意味になる。
Lot Acceptance Rate (ロット合格率):1-(1年間にその施設で不合格となったロット数を、同年の製造を手がけたロット数で割った比率)。
Right First Time Rate (直行率?):1-(1年間にその施設で少なくとも1つの逸脱を示したロット数を、同年の製造を手がけたロット数で割った比率)。
Product Quality Complaint Rate (製品品質苦情率):規格を満たさなかった医薬品の現実的または潜在的な欠陥に関する苦情の受理数を、同年の総出荷ロット数で割った比率。
Invalidated Out-of-Specification (OOS) Rate (無効OOS比率):1年間にその施設または契約施設で無効にしたOOS試験結果を、同年の試験実施回数で割った比率。
Annual Product Review (APR) on Time Rate (予定通りの年次製品照査実施率):期日の30日以内に作成された年次照査の数を、その施設で製造している製品数で割った比率。
Management Engagement(経営者の言質):以下の一人として報告された、各製品年次照査に署名した最も上位のシニアマネジメント:(1)特定されていない、(2)ラインの品質マネージャー、(3)工場長、(4)コーポレートの上級マネージャー。
Performance Question 1(質問1):製品年次照査の一つとして、その施設が各重要品質特性に関する工程能力または評価指数を計算したかいなかの「はい」「いいえ」の回答。
Performance Question 2(質問2):その施設が低い工程能力または評価指数に対するCAPAの要求方針を持っているか否かの「はい」「いいえ」の回答。
Performance Question 3(質問3):2の質問に「はい」と回答したら、CAPAの引き金になる工程能力または評価指数は何か、「いいえ」と回答したら何も対応しないこと。
Corrective and Preventative Action (CAPA) Rate (CAPA比率):製品年次照査によって開始した是正処置または予防処置(CAPA)の数を、製品年次照査の実施数で割った比率。
マネジメントレビューでチェックされるKey Performance Indicators(重要業績評価指標)なるものがある。これは、品質システムが継続して効果的に実施されていることをモニターするために定める指標だ。
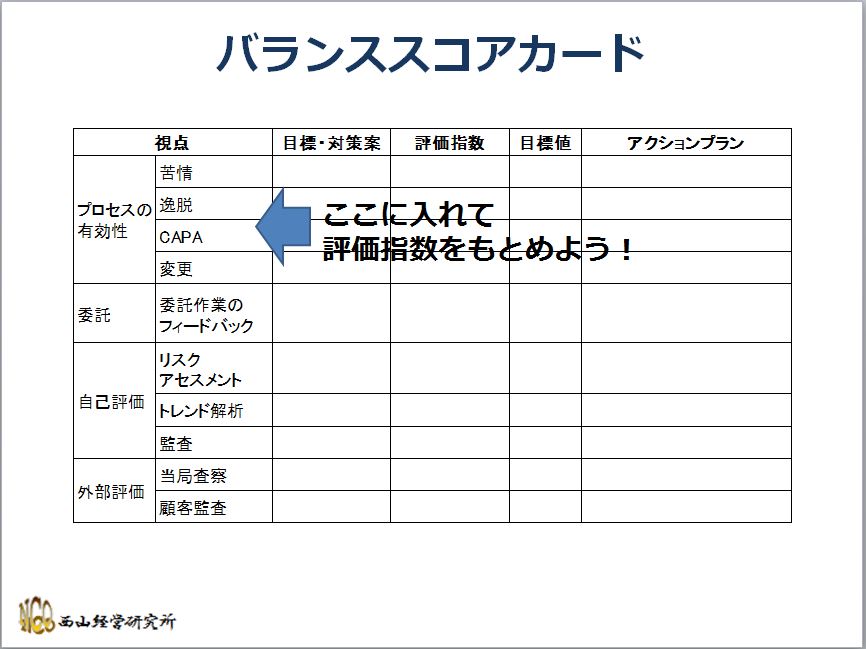
バランススコアカードのプロセスの有効性の欄に、これらを入れてモニタリングしていったらどうかな??
品質測定は、FDAが会社を評価するためのアプローチだ。以前にもリスクベースアプローチというFDAが会社を評価するためのアプローチがあった。これは、やがて業界に浸透して、別の領域で活用されるに至った経緯がある。そのうち、品質測定もそのような道をたどるのではないかな?? バランススコアカードにこれらのキーエレメントを入れておこう。
その前にしなければならないことがある。それは、マネジメントレビューが浸透することである。これが前提でなければ、あまり意味はないかもしれない。