システム査察の概要(1):システム査察の枠組み
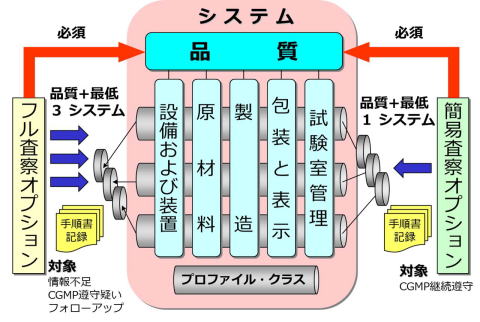
システム査察は、GMP遵守状況の評価の焦点を特定の製品から工場全体にシフトしたアプローチです。工場全体を評価することで、定期的かつ継続的な査察の低減や、承認前査察の回数と調査の深さを削減することを目的とした手法です。
工場全体をGMPの領域を6つに分類し、その領域の複数のプロファイルクラスを調査することにより、各システムの管理状態を評価するアプローチです。その評価は、FDA FACTS(Field Accomplishments & Compliance Tracking System)と呼ばれるシステムに登録され、会社のGMP遵守状態がアップデートされます。いわゆる、企業のアカウントプロファイルが作成されるわけです。
この査察が大きな話題を呼んだ背景は、これまでの査察と異なり、どれか一つのシステムにおいて重大な欠陥が観察された場合でも、工場の全行為が不適切であるとみなされるからです。いわゆる「Fatal flaw」シナリオ(致命的な欠陥シナリオ)であり、その場で査察が中止されることもあり得ます。
企業の遵守状態がよい場合には、システム査察時に品質システムと他の最低1システムを調査する簡易オプションが採用されます。遵守状態が好ましくない場合 や今まで企業の情報が不十分な場合には、品質システムと他の最低3システムを調査するフルオプションが採用されます。
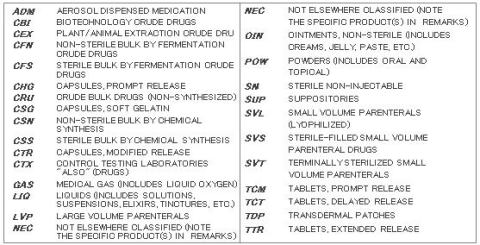
プロファイルクラス
2008年2月現在のFDAの分類
システムの概要
各 システムは、以下の査察対象項目に関する承認済み手順書と手順の実施結果の記録を有することが求められます。手順の実施は、査察中の観察によって確認され ます。査察の対象は、最終製品、原料、中間製品に及び、観察された欠陥は、他のシステムへの拡大調査につながる可能性もあります。原則として、システムの 全領域を対象とします。 また、人員への教育訓練も共通の要件となっています。
品質システム
GMP、手順、規格などの全体の遵守を保証するシステムです。このシステムは、品質部門(品質保証と品質管理試験室)とその部門が実施するレビューと承認の全てを含みます(たとえば、変更管理、再加工、バッチの出荷判定、年次照査、バリデーションプロトコルや報告書など)。
設備および装置システム
製造に用いる建物、設備、装置や、製品への組み込みを意図しないHVAC、圧縮ガス、 スチーム、水システム等のユーティリティのシステムです。建物や設備はメンテナンスを、装置は適格性の確認(IQ,OQ)、装置の校正とメンテナンス、ク リーニングとクリーニング・プロセスのバリデーションを含みます。
原材料システム
このシステムは、最終製品、製品に組み込まれる水、ガスを含む原料、容器/栓を管理する方法と活動を含む。これには、コンピュータ化した在庫管理プロセスのバリデーション、医薬の保管、物流管理および記録が含まれる。
製造システム
バッチの調合、製剤化、工程内サンプリングと試験、およびプロセス・バリデーションを含めた医薬および医薬品の製造を管理するシステムです。また、承認された製造手順の確立、順守、記録の作成も含まれます。
包装および表示システム
医薬品の包装と表示を管理するシステムです。手順書、ラベルの検査と使用、ラベルの保管と発行、包装と表示の作業管理、およびこれらの作業のバリデーションが含まれます。
試験室システム
試験検査室の手順、試験、分析方法の開発とバリデーションまたは検証(verification)安定性プログラムに関連する活動のシステムです。